行业动态首页 > 新闻动态 > 行业动态
在2013年的美国肿瘤学年会上,“免疫检查点抑制剂”药物因为具有良好的抗肿瘤效果而备受瞩目。此后,恶性肿瘤的免疫治疗开始席卷整个肿瘤治疗界,大量的临床试验迅速地开展,癌症免疫疗法也开始用于恶性肿瘤患者的治疗,越来越多的恶性肿瘤患者从中获益。
虽然癌症免疫疗法可在一些患者中持续使用多年,但也可能会造成严重的不良影响,甚至会危及生命。所以,目前我们迫切需要一种方法来区分最有可能从免疫疗法中受益的患者和会引起严重不良事件高风险的患者。
近日,美国肿瘤临床协会(ASCO)在《临床肿瘤学杂志》(Journal of Clinical Oncology)发布了《2019临床肿瘤学进展年度报告》,报告中阐述了加快推动癌症诊疗进展的九大研究方向。第一条关于确定更好地预测免疫治疗策略的重点之一是开发基于血液和组织的生物标志物;第二条关于更好地定义受益于术后(辅助)治疗患者群体的重点之一是开发具有临床效用的有效生物标志物,以确定肿瘤治疗后的复发风险,对具有不同风险程度的患者做出最佳选择。
那么,究竟什么是肿瘤免疫治疗呢?
肿瘤免疫疗法这一概念在19 世纪末被提出,指的是利用人体自身的免疫系统来消灭癌细胞的一种治疗方法。目前,治疗恶性肿瘤最具前景的免疫治疗药物是PD-1/PD-L1抑制剂。
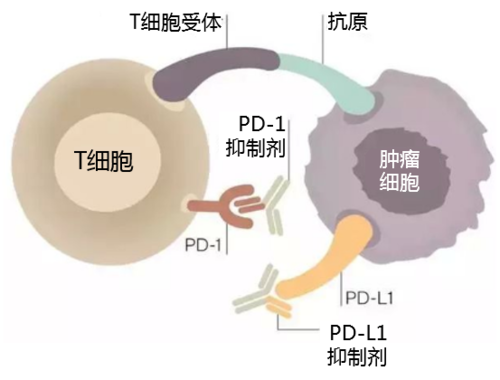
PD-1可在活化的T细胞、B细胞及髓系细胞中表达,而PD-L1在多种组织中都有表达,并在肿瘤组织中高表达。当PD-1与肿瘤表面的PD-L1结合时,活化的T细胞将无法识别肿瘤细胞,从而抑制T细胞的杀伤功能,对人体免疫应答起到负调节作用。
而PD-1/PD-L1抑制剂能够特异性地和肿瘤细胞上的PD-L1结合来抑制其表达,阻断肿瘤细胞PD-1/ PD-L1信号通路,从而能够使功能受抑制的T细胞恢复对肿瘤细胞的识别功能,让免疫系统直接杀死癌症细胞。这种免疫疗法具有针对性,能抗击多种类型的肿瘤。
PD-1/PD-L1抑制剂的优点:
1)持久性:对PD-1/PD-L1抑制剂有效的病人,疗效维持的平均时间较长。
2)广谱性:PD-1/PD-L1抑制剂对于绝大多数肿瘤都是可以尝试的,如肝癌、结直肠癌、胃癌、食管癌、三阴性乳腺癌、鼻咽癌、卵巢癌、宫颈癌等;
3)低毒性:与传统的放化疗等治疗手段相比,PD-1/PD-L1抑制剂毒副作用要小的多。
虽然PD-1/PD-L1抑制剂副作用小,但这并不意味着就毫无风险。部分患者也会出现严重的免疫相关的炎症反应,如免疫性肺炎、免疫性肠炎、免疫性肝炎、甚至免疫性心肌炎。
我们又该如何做才能有效预防免疫治疗带来的不良后果呢?
近年来,随着靶向治疗和免疫治疗方法的逐渐成熟,研究者也发现了一些用于特定癌种的预测PD-1疗效的指标,如微卫星不稳定性(microsatellite instability, MSI)和肿瘤突变负荷(Tumor Mutational Burden, TMB)。
当肿瘤细胞中存在 MMR 基因功能缺失(Mis-Match Repair deficiency,简称 dMMR)时,标志肿瘤细胞失去对 DNA 复制错误的修复能力,肿瘤细胞内将积累大量突变,就会伴随出现微卫星不稳定性(MSI)特征。研究表明,肿瘤细胞携带的突变越多,能被患者自身免疫系统特异性识别的新生抗原就越多,免疫系统特异性杀伤肿瘤细胞的概率就越大。2017 年 5 月 23 日,FDA 首次批准了 PD-1 抗体药物 Keytruda 用于「dMMR/MSI-H」型实体瘤的治疗,这是首款不依照肿瘤来源,而是依照分子标志物进行区分的抗肿瘤疗法,具有里程碑式的意义。
肿瘤突变负荷(TMB),通常以肿瘤组织每Mb碱基中发生替换和插入缺失突变的总数衡量。高TMB肿瘤,产生更多新抗原或新表位,从而更有效地激活T细胞引起免疫响应。2018年,JCO上发表的一篇研究论文,分析了240例接受PD-1抑制剂治疗的晚期肺癌患者的相关资料,得出了肿瘤突变负荷(TMB)越高的患者,疗效越好的结论(受益和非收益组比较,p value=0.006)。
但是对于免疫治疗的响应预测,这些常用的监测监测指标不尽如人意,找出机体内存在的针对特定抗原靶标的自身抗体来预测免疫治疗后不良反应的发生也许是个好方法!美国肿瘤临床协会在2019年的年度报告中也将开发基于血液和组织的生物标志物来预测免疫治疗疗效作为未来一大重点工作。如果在治疗前对患者进行相关生物标记物的检测,将有助于更好的实现精准治疗,为患者选择最为适合的治疗方案。
广州博翀生物科技有限公司拥有Huprot人蛋白质组芯片,该款芯片上含有2万多个人重组蛋白,是肿瘤生物标志物的高通量筛选工具。目前我司已为数十种疾病的早诊生物标志物提供筛选平台,均取得不错的结果。开展基于血液和组织的生物标志物来预测免疫治疗疗效这一工作,Huprot人蛋白质组芯片将为您提供便捷途径!
